Position Statement GIMBE
Evidence 2015;7(5): e1000111 doi: 10.4470/E1000111
Pubblicato: 26 maggio 2015
Copyright: © 2015 Cartabellotta. Questo è un articolo open-access, distribuito con licenza Creative Commons Attribution, che ne consente l’utilizzo, la distribuzione e la riproduzione su qualsiasi supporto esclusivamente per fini non commerciali, a condizione di riportare sempre autore e citazione originale.
I pazienti con infezione da virus dell’epatite C dovrebbero essere correttamente informati rispetto a due preoccupazioni principali (1). La prima è correlata alla storia naturale della malattia che può progredire verso forme avanzate: sviluppo di cirrosi epatica, scompenso della cirrosi, epatocarcinoma, necessità di trapianto di fegato, morte. La seconda riguarda la possibilità di prevenire l’evoluzione della malattia e dipende dall’efficacia del trattamento.
1. Storia naturale dell’epatite C
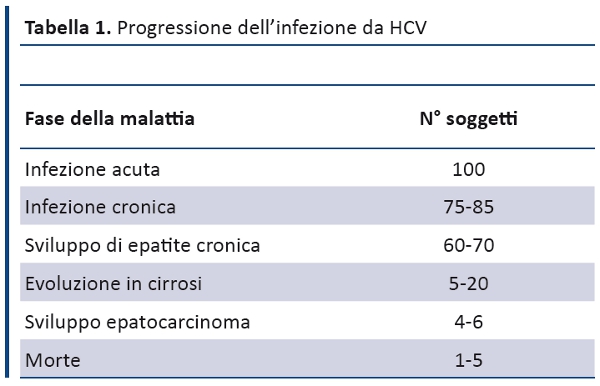
La fase acuta dell’epatite C è asintomatica nella maggior parte dei pazienti: secondo il Centers for Disease Control and Prevention (CDC) ogni 100 persone con infezione da HCV solo 20-30 sperimentano sintomi generici quali astenia, riduzione dell’appetito, nausea (2). L’evoluzione della malattia è riportata nella tabella 1, da cui emergono alcuni dati fondamentali: innanzitutto, il 30-40% dei soggetti con infezione cronica da HCV non sviluppa epatite cronica; in secondo luogo, la cirrosi si sviluppa nel 20% dei pazienti dopo una mediana di 40 anni dall’infezione; infine, la mortalità (per complicanze della cirrosi e/o epatocarcinoma) è inferiore al 5%.
2. Metodi
È stata effettuata una revisione sistematica degli health technology assessment (HTA) reports sul sofosbuvir, selezionando quelli pubblicati negli ultimi 12 mesi da agenzie governative indipendenti:
- Institute for Quality and Efficiency in Health Care (IQWiG) (3). Aprile 2014
- Institute for Clinical and Economic Review (ICER) (4). Aprile 2014
- Canadian Agency for Drugs and Technologies in Health (CADTH) (5). Agosto 2014
- NIHR Horizon Scanning Centre (6). Gennaio 2015
- Blue Cross Blue Shield Association (BCBS) (7). Gennaio 2015
- National Institute for Health and Care Excellence (NICE) (8). Febbraio 2015
La valutazione degli HTA reports è stata integrata da revisioni sistematiche identificate sulla Cochrane Library e su MEDLINE (9,10,11,12,13,14).
2.1. Limiti metodologici delle evidenze disponibili
Dall’analisi comparativa degli HTA reports inclusi nella valutazione emergono numerose criticità metodologiche rispetto alla robustezza delle prove di efficacia, oltre che all’entità dei benefici del trattamento con sofosbuvir.
- Tutti gli studi che hanno valutato l’efficacia del sofosbuvir sono stati finanziati, progettati e realizzati dall’azienda produttrice Gilead Science e, al momento, non esiste alcuno studio indipendente.
- Non conosciamo il reale valore aggiunto del farmaco rispetto a un confronto appropriato, sia perché mancano trial di efficacia comparativa del sofosbuvir con altri agenti antivirali ad azione diretta, sia perché tutti gli studi prevedono l’associazione del sofosbuvir con ribavirina ± peginterferon-alfa.
- Alcuni studi presentano limiti metodologici rilevanti (controlli storici, assenza di blinding) o prevedono un disegno di non-inferiorità.
- Tutti gli studi hanno utilizzato come misura di esito un end-point surrogato (box 1), ovvero la risposta virologica sostenuta — sustained virological response (SVR) — al di sotto della soglia minima identificabile a 24 settimane (SVR-24) o, dopo lo “sdoganamento” della FDA a 12 settimane (SVR-12) dalla sospensione del farmaco.
- La SVR non garantisce l’eradicazione del virus dal sangue (che resta solo al di sotto della soglia minima identificabile), né permette di identificare la persistenza del virus nei tessuti.
- Per alcuni sottogruppi di pazienti la stima dell’effetto del trattamento è incerta a causa della loro limitata numerosità campionaria.
- Non esistono prove di efficacia dirette su outcome clinicamente rilevanti: evoluzione dell’epatite in cirrosi, scompenso della cirrosi, insorgenza di epatocarcinoma, mortalità.
- Non è nota la probabilità di re-infezione nei pazienti che hanno ottenuto una SVR.
- Non conosciamo gli effetti avversi, oltre che la compliance, nel mondo reale.
|
Box 1. Validazione degli end-point surrogati
|
3. Raccomandazioni basate su criteri di costo-efficacia
Il report pubblicato nel febbraio 2015 dal National Institute for Health and Care Excellence (NICE), dopo una valutazione sistematica dei 13 studi presentati dalla Gilead Science ha identificato:
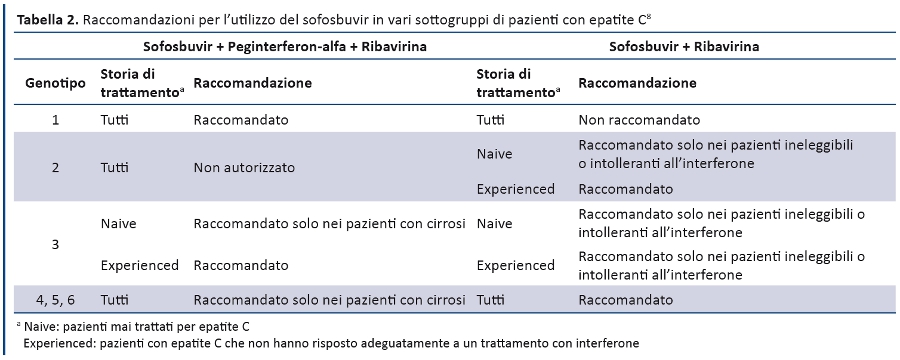
- L’efficacia del farmaco nei vari sottogruppi di pazienti (tabella 2).
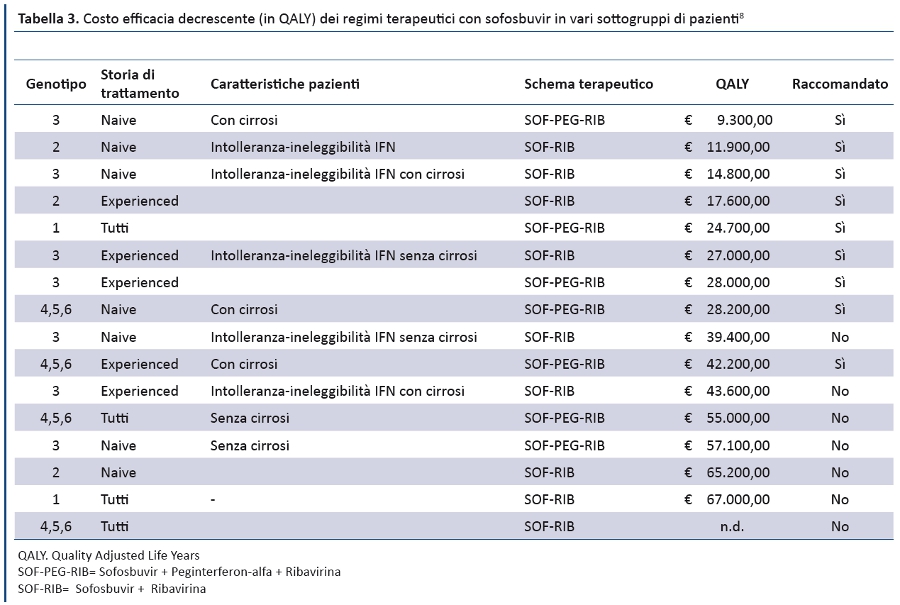
- La costo efficacia del trattamento espressa in anni di vita aggiustati per la qualità — Quality Adjusted Life Years (QALY) - offrendo un parametro oggettivo per definire le priorità dei pazienti da trattare (tabella 3).
4. Conclusioni
Il sofosbuvir costituisce una rilevante innovazione terapeutica, ma le evidenze disponibili documentano solo che il farmaco è efficace nel determinare una risposta virologica sostenuta in una percentuale che raggiunge il 90% in alcuni (ma non in tutti) sottogruppi di pazienti.
- La storia naturale dell’epatite C e le prove di efficacia disponibili non giustificano in nessun contesto sanitario, indipendentemente dalla disponibilità di risorse, una policy che preveda il trattamento di tutti i pazienti con epatite C con l’obiettivo di prevenire l’evoluzione dell’epatite cronica in cirrosi, lo scompenso della cirrosi, lo sviluppo dell’epatocarcinoma, i trapianti di fegato e la mortalità.
- In assenza di prove di efficacia dirette sulla capacità del sofosbuvir di rallentare l’evoluzione dell’epatite C verso forme avanzate di malattia, o di una robusta validazione dell’end-point surrogato SVR, scommettere sui potenziali risparmi per l’assistenza sanitaria è puramente speculativo e non supportato da alcun dato scientifico (25,26).
- Assimilare la risposta virologica sostenuta nel singolo paziente alla eradicazione del virus dell’epatite C dalla popolazione è una suggestiva, ma inverosimile, strategia di sanità pubblica.
- Considerato che la mortalità nei pazienti con epatite C è molto bassa e che nessuno studio ha dimostrato che il sofosbuvir riduce la mortalità, il termine “farmaco salvavita” è improprio e non dovrebbe più essere utilizzato.
- Definire le priorità di trattamento in relazione alla costo-efficacia del sofosbuvir nei vari sottogruppi di pazienti rappresenta oggi l’unica soluzione accettabile dal punto di vista clinico, etico ed economico.
- I dati relativi a tutti i pazienti trattati dovrebbero essere raccolti in maniera sistematica al fine di documentare l’efficacia e la sicurezza del farmaco nel mondo reale.
- Tutti gli stakeholder che intervengono pubblicamente esaltando l’efficacia del sofosbuvir, oltre le evidenze disponibili, dovrebbero dichiarare gli eventuali conflitti di interesse finanziari e non finanziari.



